Nhiệt độ sôi của benzen là gì? Khái niệm, Tính chất và bài tập là những thông tin mà chúng tôi xin gửi đến các bạn nội dung bài viết dưới đây giúp các bạn có được những kiến thức liên quan đến hợp chất hữu cơ này. Hãy tìm hiểu để có thêm kiến thức vận dụng vào bài tập cũng như thực tiễn nhé.
ĐỊNH NGHĨA , ĐỒNG ĐẲNG, ĐỒNG PHÂN, DANH PHÁP, CẤU TẠO
Định nghĩa về Benzen
Benzene là một hợp chất hữu cơ có công thức hoá học C6H6. Benzen là một hyđrocacbon thơm, trong điều kiện bình thường là một chất lỏng không màu, mùi dịu ngọt dễ chịu, dễ cháy. Benzen tan kém trong nước và rượu Vì chỉ chứa carbon và hydro nên benzene là một hydrocarbon.
Dãy đồng đẳng của benzen
Benzen C6H6 và các hiđrocacbon thơm khác có công thức phân tử là C7H8 (toluen), C8H10, lập thành dãy đổng đẳng có công thức phân tử chung CnH2n−6(n≥6).
Đồng phân, danh pháp
Một số hiđrocacbon thơm đầu dãy đồng đẳng có công thức cấu tạo và tên gọi được trình bày trong bảng
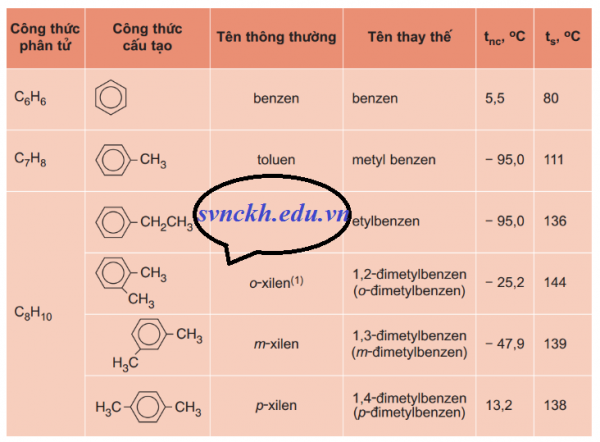
Từ C8H10 trở đi có các đổng phân về vị trí tương đối của các nhóm ankyl xung quanh vòng benzen và về cấu tạo mạch cacbon của mạch nhánh.
Tên hệ thống của các đổng đẳng của benzen được gọi bằng cách gọi tên các nhóm ankyl + benzen.
Bạn có biết : Nhiệt độ sôi của các chất
Cấu tạo
Để thể hiện cấu tạo của benzen, ngày nay người ta dùng một trong hai công thức cấu tạo sau:
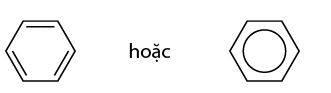
Tính chất của Benzen
Tính chất vật lý
Các hiđrocacbon thơm đều là chất lỏng hoặc rắn ở điều kiện thường, chúng có nhiệt độ sôi tăng theo chiều tăng của phân tử khối Như : C6H6 có nhiệt độ sôi là 80 độ C, C7H8 có nhiệt độ sôi là 111 độ C…
Các hiđrocacbon thơm ở thể lỏng có mùi đặc trưng, không tan trong nước và nhẹ hơn nước, có khả năng hoà tan nhiều chất hữu cơ.
Tính chất hóa học
Phản ứng cộng
a) Cộng hiđro
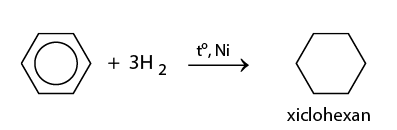
b) Cộng clo
Dẫn lượng nhỏ khí clo vào bình chứa một ít benzen, đậy kín lại rồi đưa bình ra ngoài ánh nắng. Trong bình xuất hiện khói trắng và thành bình xuất hiện một lớp bột màu trắng. Đó là 1,2,3,4,5,6-hexacloxiclohexan (hexacloran).
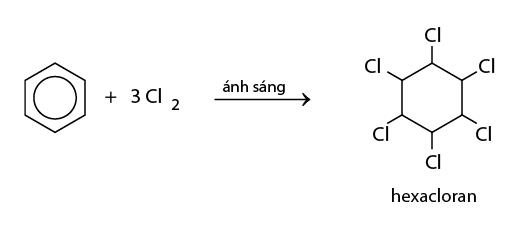
Phản ứng thế
a) Thế nguyên tử H của vòng benzen
* Phản ứng với halogen
Cho benzen và brom vào ống nghiệm khô rồi lắc nhẹ hỗn hợp.
Cho tiếp một ít bột sắt vào ống nghiệm trên, lắc nhẹ. Màu của brom nhạt dần và thấy có khí hiđro bromua thoát ra do đã xảy ra phản ứng thế:
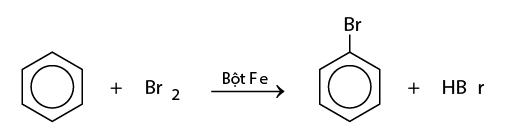
Nếu cho các ankylbenzen phản ứng với brom trong điều kiện có bột sắt sẽ thu được hỗn hợp sản phẩm thế brom chủ yếu vào vị trí para và ortho so với nhóm ankyl:
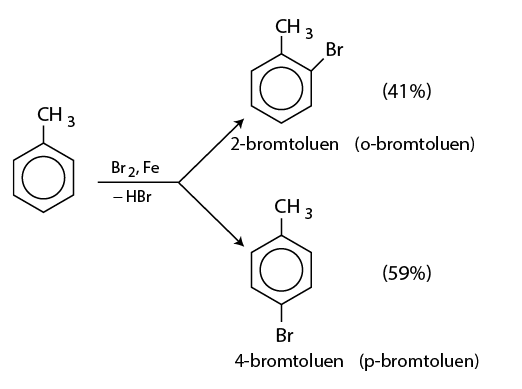
* Phản ứng với axit nitric
Cho benzen vào ống nghiệm chứa sẵn hỗn hợp H2SO4 đặc và HNO3 đặc. Khi đó sẽ thấy có lớp chất lỏng nặng màu vàng nhạt lắng xuống. Đó là nitrobenzen được tạo thành theo phản ứng:
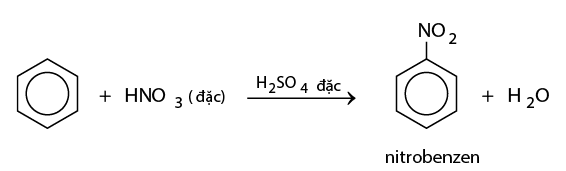
*Quy tắc thế: Các ankylbenzen dễ tham gia phản ứng thế’ nguyên tử H của vòng benzen hơn benzen và sự thế ưu tiên ở vị trí ortho và para so với nhóm ankyl.
b) Thế nguyên tử H của mạch nhánh
Nếu đun toluen hoặc các ankylbenzen với brom, sẽ xảy ra phản ứng thế nguyên tử H của mạch nhánh tương tự ankan.
Bạn có biết : Nhiệt độ sôi của ancol
Phản ứng oxi hoá
a) Phản ứng oxi hoá không hoàn toàn
Thí nghiệm:
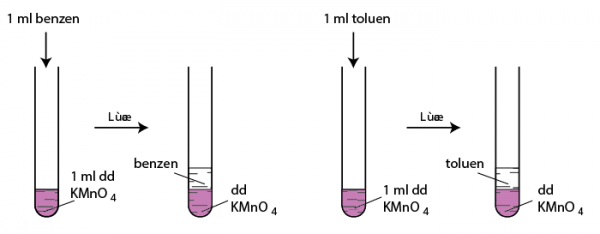
Khi đun nóng đồng thời cả hai ống nghiệm trong nồi cách thuỷ:
– Benzen vân không làm mất màu dung dịch kali pemanganat.
– Toluen làm mất màu dung dịch kali pemanganat, tạo kết tủa mangan đioxit.
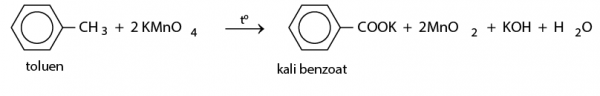
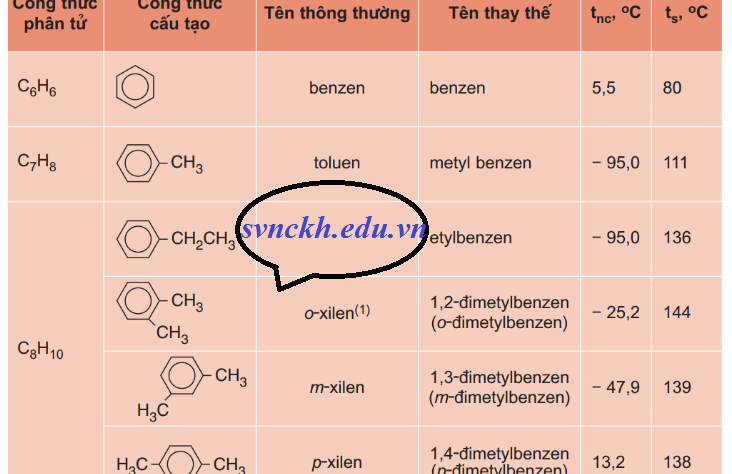
b) Phản ứng oxi hoá hoàn toàn
Các hiđrocacbon thơm khi cháy toả nhiều nhiệt: